Seit der Jahrtausendwende wächst die Zahl der veröffentlichten Publikationen zu metallorganischen Gerüstverbindungen («metal-organic frameworks», MOFs) unaufhörlich. Das wissenschaftliche Interesse scheint nicht abzuflachen. Auch die Industrie liebäugelt mit dieser vielversprechenden chemischen Verbindung. Obschon die grosse Massenproduktion noch ausgeblieben ist, geben sich viele sicher: Ihre grosse Stunde wird schon noch schlagen.
In der stofflichen Welt gilt eine verblüffend einfache Faustregel: Die Struktur eines Moleküls verrät uns sofort, wozu die Verbindung in der Lage ist. Bei den metallorganischen Gerüstverbindungen («metal-organic frameworks», MOFs) verhält es sich nicht anders. Etwa 2 Gramm dieses Materials verfügen über eine Gesamtoberfläche, die mindestens so gross ist wie ein Fussballfeld. Das Potenzial dieser hochporösen Moleküle lässt sich nur schon durch diesen Vergleich erahnen.
Bekannt für seine Gastfreundschaft
Als Entdecker der MOFs gilt der Chemiker Omar M. Yaghi. 1995 veröffentlichte er zusammen mit seinem Team den ersten stabilen MOF in der Fachzeitschrift «Nature»: An das Metallzentrum Co(II) koordiniert mehrfach die organische Verbindung Trimesinsäure (BTC) in ihrer deprotonierten Form. So gesehen, handelt es sich um eine gewöhnliche Komplexverbindung mit BTC als Liganden. Was macht nun aus diesem Komplex ein MOF?

Ein einzelner Ligand verbindet sich gleich mit mehreren Metallzentren und diese wiederum gehen mit neuen Liganden weitere Verbindungen ein: Ein zweidimensionales Metall-Ligand-Netzwerk entsteht. Dieser zusammengewobene Teppich aus Komplexverbindungen wird vertikal erweitert: Ein zusätzliches Molekül, in diesem Fall Pyridin, verknüpft nun diese metallorganischen Schichten miteinander, indem es sich mit den Metallen verbindet. Wie bei einem Hochhaus werden so Stockwerk für Stockwerk aufeinandergestapelt. Zwischen jeder Etage dieser Metall-Ligand-Netzwerke bilden sich grosse Hohlräume. Dank diesen weisen MOFs eine so hohe spezifische Oberfläche auf und können «Gastmoleküle» empfangen, speichern und wieder freigeben, ohne dass die wabenartige Struktur der MOFs verloren geht.
Und genau das haben Yaghi und sein Team in diesem Paper gezeigt. Sie konnten das metallorganische Gerüst mit Molekülen beladen und entladen, ohne dass die Struktur der MOFs in sich zusammengebrochen wäre.
Molekulare Legosteine
Solche Eigenschaften sind allerdings nichts neues in der Chemie. Gerade die Stoffklasse der Zeolithe zeichnet sich durch ihre hohe spezifische Oberfläche aus. Doch MOFs sind aus chemischer Sicht trickreicher. Da das Gerüst aus organischen Liganden besteht, lässt sich das Gebilde nämlich «dehnen» oder «verdichten». Auch die Bestandteile des Materials lassen sich variieren. Ein anderes Metallzentrum oder andere organische Liganden mit neuen funktionellen Gruppen lassen sich integrieren. Die Chemikerin oder der Chemiker kann also die Eigenschaften der MOFs bis ins kleinste Detail modifizieren.
Industrie zeigt waches Interesse
1999 stellten Yaghi und sein Team einen neuen Rekord auf. Sie synthetisierten einen MOF, der so löchrig ist wie kein Stoff vor ihm. Sie nannten das neue Material MOF-5 (Zn4O(BDC)3) und es sollte das bekannteste und am besten untersuchte MOF werden.
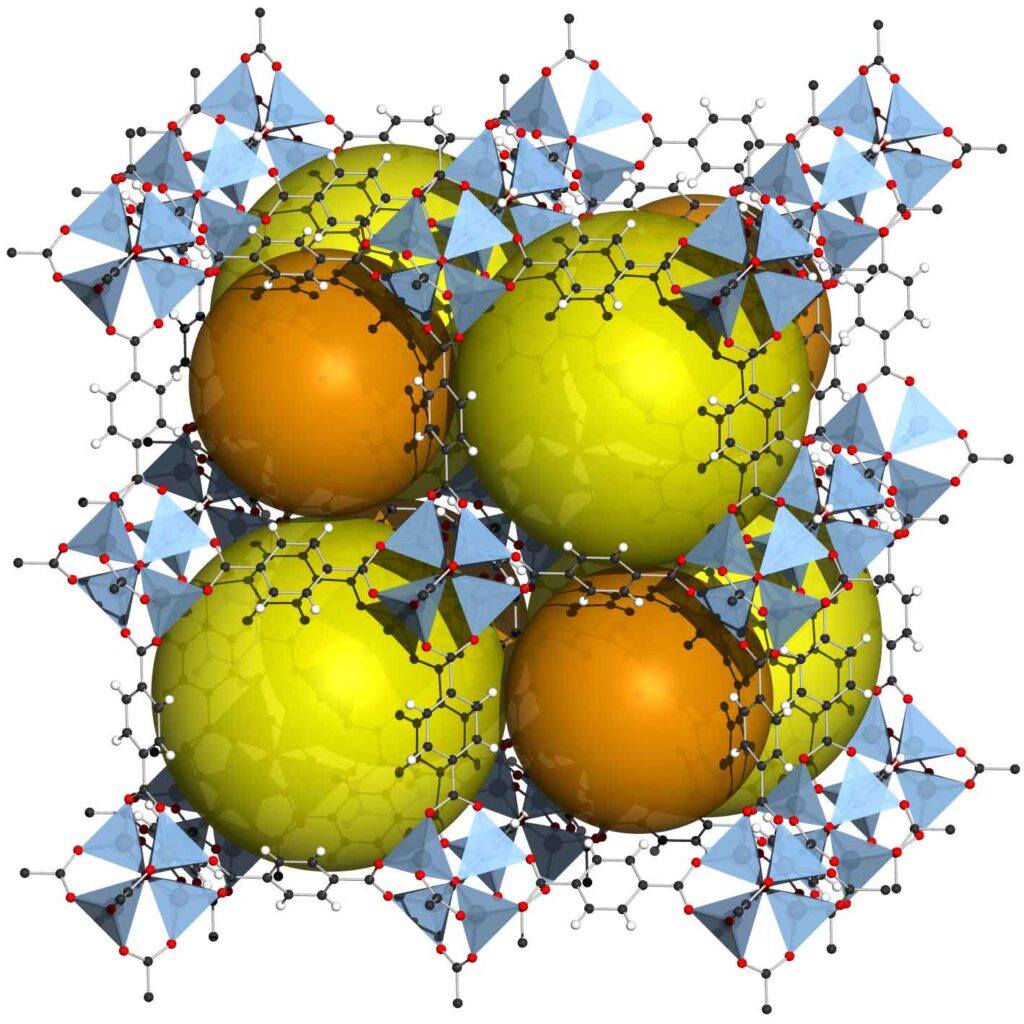
MOF-5 (Bild 3) weist eine massenbezogene spezifische Oberfläche von ungefähr 3000 m2/g auf. Es dauerte nicht lange und die Fachwelt wurde hellhörig. Ein Material, das über eine höhere Adsorptionsfähigkeit pro Masse verfügt als Zeolith und sich zusätzlich wie ein Baukasten ganz präzise zusammenstellen lässt, imponiert. Die technischen Potenziale, die in diesen Materialien schlummern, sind offensichtlich. So kam es, dass auch die Industrie ein reges Interesse an diesen Verbindungen zeigte: allen voran die BASF.
Der deutsche Konzern soll rund 2,5 Prozent aller MOF-Patente erworben haben. Kein anderes Unternehmen oder Organisation besitzt so viele MOF-Patente wie die BASF. Unter dem Markennamen «Basolite» produziert und verkauft der Konzern kleine Mengen unterschiedlicher MOFs.
Hoffnungsträger oder Zeitverschwender?
Doch wem dienen nun die MOFs – ausser forschungseifrigen Chemikern? Wofür kann man sie konkret anwenden? Mögliche Einsatzbereiche gibt es viele (siehe Tabelle 1). Angestellte der BASF arbeiten zum Beispiel seit Jahren an MOFs, die in der Lage sein sollen, Unmengen an Erdgas in kleinstem Raum zu speichern. Diese MOFs können dann in Tanks von Erdgas-Fahrzeugen zum Einsatz kommen. Prototypen gibt es bereits.
| Themengebiet | Konkrete Anwendungsbereiche |
| Energie und Mobilität | Gasspeicherung, Latentwärmespeicher |
| Stofftrennung | Chromatographie, Gasreinigung, Trennverfahren (z. B. CO2) |
| Katalyse | Photokatalyse, enantiosekeltive Katalyse, heterogene Molekularkatalysatoren |
| Sensorik | Raumluftqualität, optische Sensorik, Schwellenwertsensorik |
Auch für andere Gase können MOFs als Zwischenspeicher dienen, da sie schliesslich die Speicherkapazität erhöhen (hohe Energiedichte) und dadurch die Energieeffizienz steigern und Kosten senken. Es ist also gut nachvollziehbar, dass die BASF Methangas für den Einsatz im Automobilbereich mittels MOFs speichern möchte.
Wegen der grosszügigen Aufnahmefähigkeit der MOFs von Gastmolekülen sind sie prädestiniert für allerlei Trennverfahren in der Industrie. In einem neueren Projekt sammeln Forschende gar Wasser aus der Luft in Wüstengebieten, um dieses kostbare Gut schliesslich als Trinkwasser aufzubereiten.
Man könnte auch die Emission von Treibhausgasen direkt reduzieren, indem MOFs das CO2-Gas aufnehmen. Oder indirekt, indem sie Energie reduzieren, wenn sie weniger effiziente Trennverfahren in der Industrie ersetzen.
MOFs sind also Stoffe, die dabei helfen könnten, «den Planeten zu retten», wie einige junge Wissenschaftler in der Fachzeitschrift «Angewandte Chemie» tatsächlich zu formulieren wagten.
Fragt man allerdings den Entdecker der MOFs Professor Yaghi, was er von den «weltrettenden» Möglichkeiten dieser chemischen Verbindung hält, so räumt er ein, dass ihm eigentlich immer nur die Schönheit der Moleküle und nicht etwa ihr Potenzial interessiert habe. Was natürlich nicht heisst, dass er die Möglichkeiten dieser molekularen Legosteine nicht schätzen würde.
Wo bleibt der «Durchbruch»?
MOFs werden bis heute noch nicht massenhaft produziert. In bestimmten Nischenbereichen haben sich diese speziellen Verbindungen bereits festgesetzt. Nach Einschätzungen von Prof. Jürgen Caro, der sich schon seit Jahren mit MOFs beschäftigt, werde die Kommerzialisierung der MOFs in kleinen Schritten voranschreiten, wie er in einem Review schreibt. Zuerst werden die Moleküle Bereiche wie Gasspeicherung oder Anwendungen in der Sensorik erobern. Je erfolgreicher sich diese MOFs dann zeigen, desto eher werden sie im grösseren Massstab in der Trenntechnik oder Katalyse eingesetzt.
Roger Bieri




