Forschende der Universität Bern und des japanischen Forschungsinstituts Riken schicken sich an, auf zwei weit verbreiteten Metallen eine ökonomisch günstige und nachhaltige (Metall-)Organische Synthesechemie aufzubauen: Natrium und Eisen.
Alkalimetalle und Erdalkalimetalle können die Triebkraft für organische Reaktionen liefern, doch nicht alle von ihnen sind gut verfügbar. Insbesondere Lithium spielt jetzt in der Herstellung von Batterien für Elektrofahrzeuge eine tragende Rolle und wird damit seltener und teurer. Natrium dagegen ist in der Natur häufig und billig – die Alternative der Wahl, oder?
Zu schlechte Ausbeuten – schwer kontrollierbare Reagenzien
Warum sich nicht alle organischen Chemiker auf Natrium stürzen, verdeutlicht ein Blick in die Historie: Mit der Wurtz-Reaktion und der daraus entwickelten Wurtz-Fittig-Reaktion aus dem 19. Jahrhundert konnte man, unter dem Einfluss von Natrium, halogenierte Kohlenwasserstoffe miteinander verbinden. Möglich waren Homokupplungen, zum Beispiel so: Aus zwei Halogenalkanmolekülen mit der Formel CH3-(CH2)n-X wird ein doppelt so langes Kohlenwasserstoffmolekül mit der Formel CH3-(CH2)2n-CH3. In einigen Fällen funktioniert das gut, beispielsweise bei der Herstellung zyklischer Alkane: Aus Br-(CH2)6-Br wird durch eine intermolekulare Wurtz-Reaktion Cyclohexan [1]. Und mit Magnesium, anstelle von Natrium, gelingt die Synthese von Squalen. Diese Zwischenstufe der Steroid-Herstellung war zunächst als Naturstoff von den Japanern Tsujimoto und Kimura aus dem Lebertran von Walen isoliert worden, worauf unter anderem Karrer und Helfenstein im Schweizerischen Journal «Helvetica Chimica Acta» hingewiesen haben [2].
Darüber hinaus konnten auch Heterokupplungen durchgeführt werden, wie bei der Wurtz-Fittig-Reaktion. Ein Alkylhalogenid reagiert mit einem Arylhalogenid zum Alkylaromaten, etwa mit einem Alkylbenzol: CH3-(CH2)n-X + Y-C6H5 → CH3-(CH2)n-C6H5. Das Alkalimetall dient dazu, im ersten Schritt das Arylhalogenid zum Carbanion zu reduzieren; dieses negativ geladene Teilchen ersetzt im nächsten Schritt das Halogenid des Arylhalogenids.
Bei Reaktionen dieses Typs mit natriumorganischen Ausgangsverbindungen zeigten sich allerdings oft Nachteile: Die Reaktion verlief nur langsam, die Ausbeute liess zu wünschen übrig, und es drohten stets Nebenreaktionen.
Günstige Katalysatoren finden – ein Sport
In solchen Fällen hilft oft ein Katalysator. Er senkt die Aktivierungsenergie und macht auf diese Weise viele Reaktionen überhaupt erst möglich bzw. wirtschaftlich. Doch die Katalysatoren selbst stellen häufig einen erheblichen Kostenfaktor dar oder sind schwer zu beschaffen, und so wird es geradezu zu einem Sport, bei einem gegebenen Verfahren eine günstigere Alternative zu finden.
Zum Beispiel erfordert die Herstellung von «grünem Wasserstoff» heute nicht nur einen hohen Energieaufwand, sondern auch kostspielige Katalysatoren aus Edelmetallen, meist aus der Platingruppe.
Eine geeignete Alternative könnte in Übergangsmetall-Katalysatoren auf der Basis von Kobalt und Mangan liegen. Sie haben sich als effektiv und langzeitstabil erwiesen. Auch mechanistisch ist man bereits weit genommen. Wenn Mangan in einer Spinell-Geometrie im Kristallgitter des Kobalt-Katalysators vorliegt, lagert es sich während des elektrischen Spaltungsprozesses der Wassermoleküle aus dem Spinellgitter aus und nach der Wasserspaltung wieder in seine Gitterposition ein.
Dies stellt eine Idealsituation dar: Man kennt eine günstigere Alternative zu bisherigen Katalysatoren, und das Wissen um den Reaktionsmechanismus sollte gezielte Weiterentwicklungen erleichtern.
Ein klassisches Beispiel betrifft die Ziegler-Natta-Katalysatoren zur Polymerisation von Ethylen zu längeren α-Olefinen. Gelang sie zuerst mit dem seltenen und teuren Lithiumhydrid, so erwies sich später das leicht verfügbare und kostengünstige Aluminiumhydrid als der geeignetere Katalysator.
Weitere Experimente mit verschiedenen Übergangsmetallen der 4., 5. und 6. Gruppe des Periodensystems sowie mit Thorium und Uran ergaben, dass sich aus Titanverbindungen die effektivsten Polymerisationskatalysatoren herstellen liessen. Aktuelle Ziegler-Natta-Katalysatoren bestehen meist aus einem Komplex zweier Komponenten: typischerweise aus Titan(III)chlorid und Diethylaluminiumchlorid als Co-Katalysator oder Titan(IV)chlorid und Triethylaluminium.
Zurück zu den natriumorganischen Verbindungen: Beim Auffinden eines geeigneten Katalysators kommt eine weitere Herausforderung hinzu, selbst wenn es sich bei der Wurtz- bzw. Wurtz-Fittig-Reaktion teilweise anders verhielt. Im Allgemeinen gelten natriumorganische Reagenzien als hochreaktiv und schwer kontrollierbar. Auch deswegen kamen sie bei der Organischen Synthese selten zum Einsatz, insbesondere nicht in Kombination mit Übergangsmetall-Katalysatoren.
Welcher Übergangsmetall-Katalysatoren könnte sich dennoch für natriumorganische Reagenzien und ihre Reaktionen eignen?
Die Lösung lautet: Eisen
Nach den aktuellen Forschungsergebnissen aus der Kooperation zwischen der Universität Bern und dem japanischen Riken-Institut mit Niederlassungen in Tokyo und verschiedenen anderen japanischen Städten klingt die Antwort verblüffend einfach: Ein idealer Katalysator ist Eisen, das häufigste Metall auf der Erde und noch dazu besonders kostengünstig.
Mit der Kombination Natrium/Eisen lassen sich sowohl Homokupplungsreaktionen (Reaktion zweier identischer Moleküle) als auch Kreuzkupplungsreaktionen (Reaktion zweier unterschiedlicher Moleküle) durchführen. Ebenso haben die Wissenschaftler Erkenntnisse über den Ablauf der Reaktion auf molekularer Ebene gewonnen [3]: Mechanistische Untersuchungen, die auf der Herstellung und Charakterisierung von vermuteten eisenorganischen Zwischenstufen basieren, zeigen: In einer zweizähnigen Additionsverbindung (Verbindung mit zwei Koordinationsstellen) sind sowohl ein Natriumteilchen als auch ein Eisenteilchen (dieses als Zentralatom) koordiniert. Zusammen übern sie zusammen die Kontrolle über die katalytische Reaktivität.
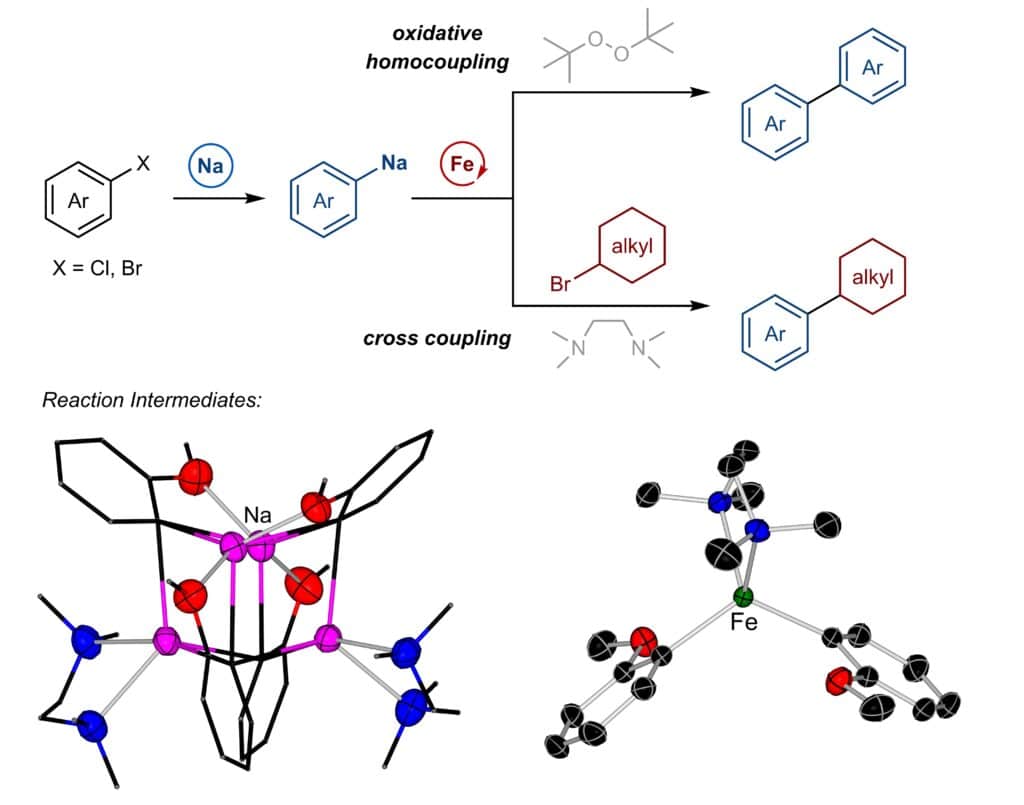
Das Wissen um den Reaktionsmechanismus bietet Möglichkeiten, das Potenzial des «Dream-Teams» Na/Fe in Zukunft noch besser auszuschöpfen. Darauf basierende nachhaltige metallorganische Reagenzien könnten in der Organischen Synthese der Zukunft eine grössere Rolle spielen. Dies eröffnet nicht zuletzt deswegen grosse Chancen, weil ein erheblicher Teil von chemischen Synthesen und von Verfahren zur Arzneimittelherstellung auf katalytischen Reaktionen beruht. Würden sie «en gros» auf Natrium/Eisen-Verfahren umgestellt, ergäbe das eine neue (Metall-)Organische-Synthese-Welt.
Dr. Christian Ehrensberger
Literatur
1. https://de.wikipedia.org/wiki/Wurtzsche_Synthese, Zugriff am 19.4.2025
2. P. Karrer u. A. Helfenstein: Synthese des Squalens. Helv. Ch. Acta 14(1) (1931): 78-85. https://doi.org/10.1002/hlca.19310140107
3. Ikko Takahashi, Andreu Tortajada, David E. Anderson, Laurean Ilies, Eva Hevia, Sobi Asako: Iron-catalysed direct coupling of organosodium compounds. nature synthesis. https://doi.org/10.1038/s44160-025-00771-1, Zugriff am 19.4.2025




