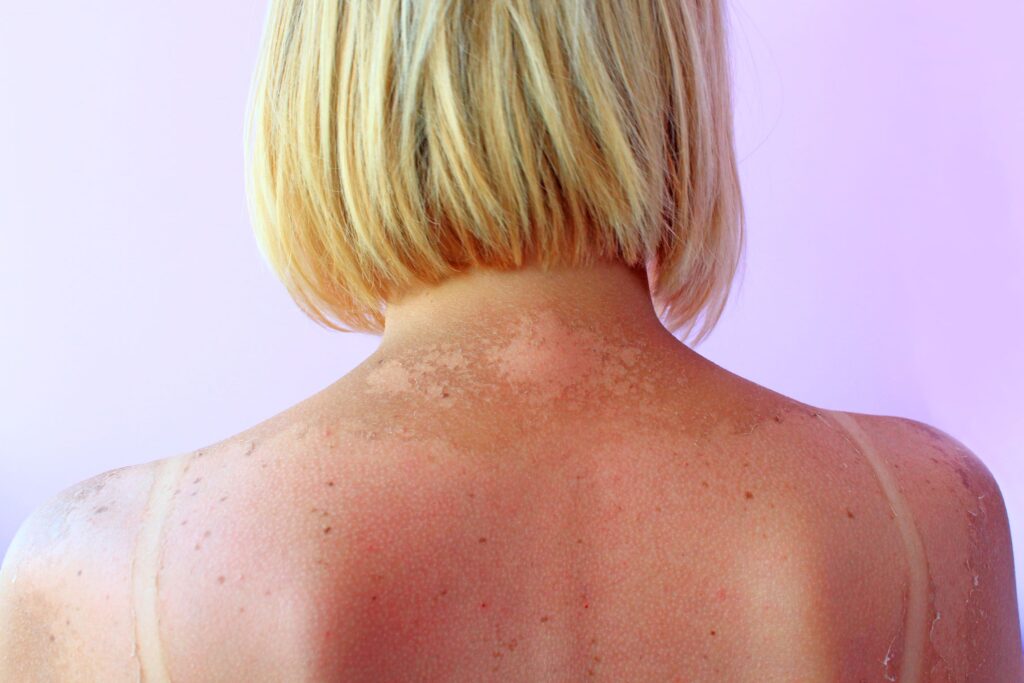
Sonnenbrand wird traditionell auf UV-induzierte DNA-Schäden zurückgeführt. Eine Studie der Universität Kopenhagen und der Nanyang Technological University (NTU), Singapur, zeigt jetzt, dass aber RNA – ein weiteres lebenswichtiges Zellmolekül – eine wichtige Rolle bei der Auslösung von akuten Sonnenbrandreaktionen spielt.
Wie wir alle wissen, sollten wir im Sommer die direkte Sonne meiden, Schatten aufsuchen, Sonnencrème anbringen oder einen Hut aufsetzen. Trotzdem haben die meisten schon einmal einen Sonnenbrand erlitten. Die Haut wird knallrot, fühlt sich gereizt an und braucht Kühlung.
Vielleicht haben Sie auch schon gehört, dass Sonnenbrand die DNA schädigt. Aber das ist nicht die ganze Wahrheit, erklären die Forschenden, die eine Studie an der Universität Kopenhagen und der Nanyang Technological University in Singapur durchgeführt haben.
«Sonnenbrand schädigt die DNA, was zu Zelltod und Entzündungen führt. So steht es in den Lehrbüchern. Doch in dieser Studie haben wir überraschenderweise erfahren, dass die akuten Auswirkungen des Sonnenbrands durch eine Schädigung der RNA, und nicht der DNA, verursacht werden», sagt Assistenzprofessorin Anna Constance Vind von der Fakultät für zelluläre und molekulare Medizin an der Universität Kopenhagen.
Die RNA ist der DNA ähnlich, aber während die DNA langlebig ist, ist die RNA ein flüchtigeres Molekül. Eine Art von RNA, die sogenannte Boten-RNA (mRNA), fungiert als zwischengeschalteter «Bote», der Informationen von der DNA zur Herstellung von Proteinen – den Grundbausteinen von Zellkomponenten – weiterleitet.
«DNA-Schäden sind schwerwiegend, da die Mutationen an die Nachkommen der Zellen weitergegeben werden, während RNA-Schäden ständig auftreten und keine dauerhaften Mutationen verursachen. Daher glaubten wir früher, dass die RNA weniger wichtig ist, solange die DNA intakt ist. Tatsächlich sind es aber Schäden an der RNA, die als erstes eine Reaktion auf UV-Strahlung auslösen», erklärt Vind.
Die Studie wurde sowohl an Mäusen als auch an menschlichen Hautzellen durchgeführt. Ziel war es, die Auswirkungen von UV-Strahlung auf die Haut zu beschreiben und die Ursachen für diese Schäden zu ermitteln. Die Forschenden fanden heraus, dass die Haut sowohl bei Mäusen als auch bei menschlichen Zellen in gleicher Weise auf UV-Strahlung reagiert.
Eingebautes Überwachungssystem für RNA-Schäden
mRNA-Schäden lösen eine Reaktion in Ribosomen aus (Proteinkomplexe, welche die mRNA «lesen», um Proteine zu synthetisieren), die von einem als ZAK-alpha bekannten Protein orchestriert wird – die sogenannte ribotoxische Stressreaktion –, wie die neue Studie zeigt. Diese Reaktion kann als ein Überwachungssystem innerhalb der Zellen beschrieben werden, das die RNA-Schäden registriert, was zu Entzündungssignalen und zur Rekrutierung von Immunzellen führt, die dann eine Entzündung der Haut auslösen.
«Wir haben herausgefunden, dass die Zellen nach einer UV-Bestrahlung als erstes auf eine RNA-Schädigung reagieren und dass dies den Zelltod und die Entzündung der Haut auslöst. Bei Mäusen, die UV-Strahlung ausgesetzt waren, fanden wir Reaktionen wie Entzündungen und Zelltod. Doch wenn wir das ZAK-Gen entfernten, verschwanden diese Reaktionen, was bedeutet, dass ZAK eine Schlüsselrolle bei der Reaktion der Haut auf UV-induzierte Schäden spielt», sagt Professor Simon Bekker-Jensen von der Fakultät für Zellular- und Molekularmedizin an der Universität Kopenhagen.
Er fügt hinzu: «Man könnte demzufolge sagen, dass alles von dieser einen Reaktion abhängt, welche alle stattfindenden Proteinübersetzungen überwacht. Die Zellen reagieren auf die RNA-Schäden und stellen fest, dass etwas nicht stimmt, was dann zum Zelltod führt.»
Schnellere und effektivere Reaktion
Das Ergebnis der in der Fachzeitschrift Molecular Cell veröffentlichten Studie verändert unser Verständnis von Sonnenbrand und den Abwehrmechanismen der Haut: dass RNA-Schäden eine schnellere und wirksamere Reaktion auslösen und die Haut vor weiteren Schäden schützen.
«Die Tatsache, dass nicht die DNA die erste Reaktion der Haut auf UV-Strahlung steuert, sondern etwas anderes, und zwar effektiver und schneller, ist ein ziemlicher Paradigmenwechsel», ergänzt Vind. «Wir müssen die Funktion der RNA-Schäden verstehen, denn das könnte langfristig unsere gesamte Herangehensweise an die Vorbeugung und Behandlung von Sonnenbrand verändern.»
Viele entzündliche Hautkrankheiten werden durch Sonneneinstrahlung verschlimmert. «Wenn wir also verstehen, wie unsere Haut auf zellulärer Ebene auf UV-Schäden reagiert, öffnet das die Tür zu innovativen Behandlungen für bestimmte chronische Hautkrankheiten», sagt Mitautor Dr. Franklin Zhong, Nanyang Assistant Professor an der Lee Kong Chian School of Medicine der NTU.
«Dieses neue Wissen stellt die Dinge auf den Kopf. Ich denke, dass die meisten Menschen Sonnenbrand mit DNA-Schäden in Verbindung bringen; das ist eine etablierte Erkenntnis. Aber jetzt müssen wir die Lehrbücher neu schreiben, und das wird sich auf die künftige Forschung über die Auswirkungen von UV-Strahlung auf die Haut auswirken», so Simon Bekker-Jensen abschliessend.